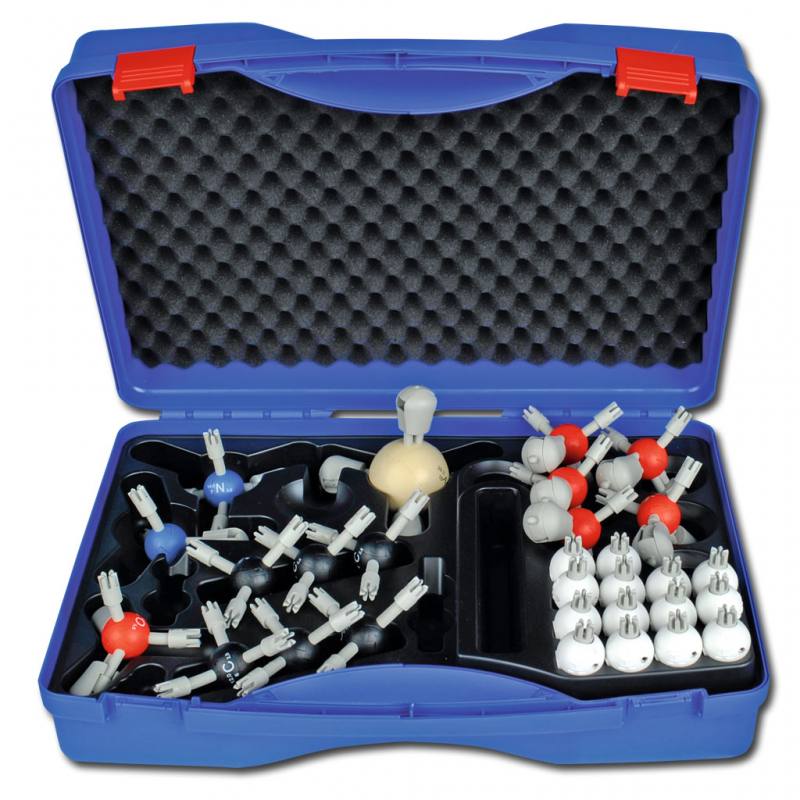
Toytomics Molekülbaukasten - Basis-Set
Art.-Nr. W-72146
- chemische Lewis-Formeln
- Struktur-Formel
- Spiel & Spaß
- periodische Eigenschaften der Elemente
- Orbitalmodelle Atombau
- Versuchserklärung
- Gruppenarbeit
- Reaktionsmechanismen
"Chemie spielerisch begreifen ..."
Toytomics Molekülbaukasten - Basis-Set
Die zentrale Rolle des Toytomics Valenzelektronenmodells
Endlich können Schüler Atome, Elektronen und Protonen anfassen und Chemie "begreifen". Wenn Schüler Reaktionen mit dem Toytomics-Atomen durchspielen, dann erschließen sich ihnen automatisch auch sämtliche andere Aspekte derselben Reaktion:
Die Lewis-Formeln mit allen Ladungen und Kräften kann man jederzeit aus dem Modell ableiten und abzeichnen. Die Strukturformeln der beteiligten Moleküle stellen sich immer richtig dar. Der Reaktionsmechanismus kann mit den Toytomics-Atomen durch spielerisches Ausprobieren exploriert werden und dadurch dann besonders gut verstanden und behalten werden (Gruppenarbeit).
Die periodischen Eigenschaften der Elemente werden automatisch klar, da jederzeit offensichtlich ist, dass z.B. Sauerstoff und Schwefel gleiche Valenzelektronen haben. Der tetraedrische Aufbau der Valenzelektronen gibt einen direkten Hinweis auf den Atombau mit Orbitalen. Durchgeführte Versuche können mit dem Modell auf der Molekülebene durchgespielt und anschaulich erklärt werden. Durch diese Möglichkeiten wird die Arbeit des Lehrers erleichtert.
Vorteile durch Toytomics
- starke Vereinfachung des Unterrichts
- chemische Formeln, Moleküle, Atome und deren Reaktionen werden einfach verstanden
- sämtliche Bindungen, Kräfte und Ladungen sind zum ersten Mal anschaulich dargestellt
- Lernen läuft visuell, haptisch und spielerisch ab
- ein Modell führt den Schüler als strukturierter roter Faden durch die Chemie
Einsatzbereiche Toytomics
- Chemieunterricht 7.-13. Klasse
- kombinierbar mit allen Unterrichtsformen und Lehrmaterialien
- sämtliche relevante Reaktionen sind darstell- und modellierbar
Inhalt
- kleiner Kasten
- 14 H, 6 C, 2 N, 6 O, 1 Ar
- Arbeitsblätter zu Anwendungsbeispielen
Anwendungsbeispiele
- Luftmoleküle: N2, O2, Ar, CO2, H2O
- Reaktionen: Knallgas, Brennstoffzelle
- Verbrennung: Kohlenstoff, Methan
- Elektronenstrichformeln: Mehrfachbindungen, Benzol, Radikale, Ionen, freie Elektronenpaare
- Organische Moleküle: Kohlenwasserstoffe, Alkohole, Aldehyde
- Carbonsäuren: Fettsäuren, Protolyse, Oxoniumion, Decarboxylierung, Ölentstehung
- Ammoniak: basische Eigenschaften, Ammoniumion
- Neutralisation: OH- und H+ zu Wasser
- Zucker: Isomere, Konfomere, Acetalbildung, Köhlerprozess, Kohleentstehung
- Fischer Projektion: Rotamere, "saggered", "eclipsed"
- Wasserstoffbrücken, Löslichkeit: hydrophil, lipohil
- CO2: Kohlensäure, Hydrogencarbonat, Carbonat
- Stickoxide: NO-, NO2-Radikal, Salpetersäure, Zwitterion, Oktettregel, Nitrat
- Radikalische Reaktionen, z.B. mit H2O2, HO, NO, NO2, Polymerisation, Ethylen
- Mesomere Grenzformeln, z.B. CO, Ozon, NO2, Benzol, Sauerstoff bi-radikal
Warnhinweise
Aufsicht von Erwachsenen
ACHTUNG! Benutzung unter unmittelbarer Aufsicht von Erwachsenen.